Panorama da geoquímica do boro (B)
O boro tem duas formas de isótopos estáveis (10B, 11B), assim como 13 formas de isótopos radioativos (de 7B a 21B, excluindo-se as formas estáveis). As formas estáveis de boro são os únicos isótopos que ocorrem naturalmente, sendo que 10B compõe 20% do boro natural e 11B compõe 80%.
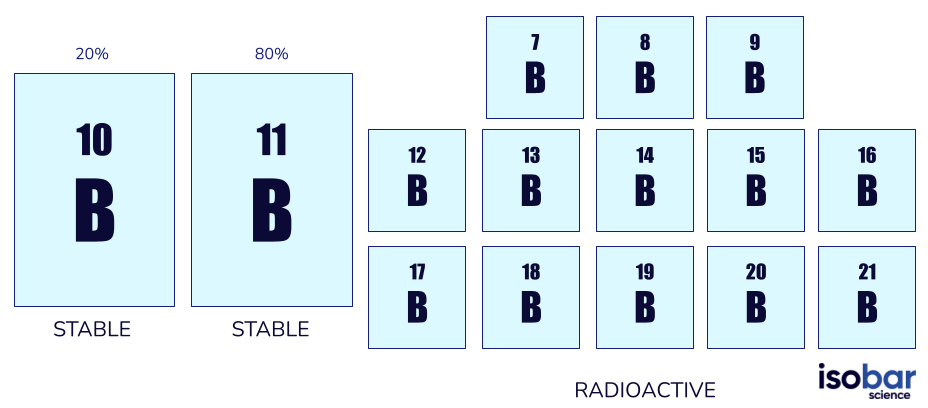
As duas espécies isotópicas de boro normalmente empregadas em estudos geoquímicos (à esquerda) e as outras 13 espécies isotópicas radioativas de boro (à direita)
Os diferentes materiais dos sistemas da terra e as condições ambientais são caracterizados por faixas distintas da razão isotópica do boro. Portanto, esse parâmetro é extensivamente usado no mapeamento geoquímico, rastreamento de fonte, previsão de contaminação, ciclos globais de carbono e estudos de circulação dos oceanos.
Mais informações em Tipos e seleção de amostras para a análise de boro.
Aviso legal: este vídeo está hospedado em um site de terceiros e poderá conter publicidade.
Esse vídeo é parte do webinar do Beta Analytic: Boron Isotopic Analysis
Paleoclimatologia e paleoceanografia
O boro dissolvido em água marinha aparece primariamente na forma de duas espécies mononucleares, o ácido bórico (H3BO3 ou B(OH)3) e o borato (BO3-3 ou B(OH)4−), com fracionamento distinto entre as duas espécies, de forma que o ácido bórico é enriquecido no isótopo mais pesado (11B) por 27,2%. A proporção relativa dessas espécies depende do pH, como ilustrado abaixo:
B(OH)3 + H2O ↔ B(OH)4− + H+
pH alto ↔ pH baixo
O boro é incorporado aos carbonatos biogênicos e inorgânicos primariamente como as espécies de borato. Porém, as espécies e concentrações particulares do boro incorporado aos carbonatos biogênicos (como conchas) dependem do pH. Dessa forma, a composição isotópica do boro de carbonatos marinhos biogênicos reflete o pH da água marinha.
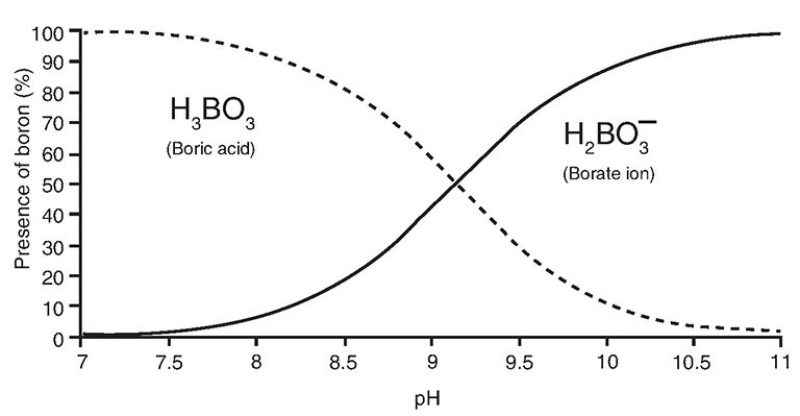
A relação entre pH e porcentagem de duas espécies diferentes de boro (https://jpt.spe.org/comparison-methods-boron-removal-flowback-and-produced-waters)
Leia mais em nosso blog:
Mapeamento geoquímico e detecção de fonte de contaminantes
O boro é amplamente usado na indústria (lubrificantes, fundentes, aditivos), na agricultura (micronutriente de fertilizantes) e no ambiente doméstico (agente clareador). O boro é um importante aditivo na fabricação do aço para aumentar a temperabilidade de um material. Por exemplo, aços de boro são empregados extensivamente na indústria nuclear para proteger sistemas e controlar reações nucleares, devido à sua habilidade natural de absorver nêutrons. Em outras indústrias, um composto de boro conhecido como borato de sódio (“Borax”) é largamente usado em detergentes para a remoção de manchas e limo, assim como em produtos cosméticos como conservante e agente tamponador.
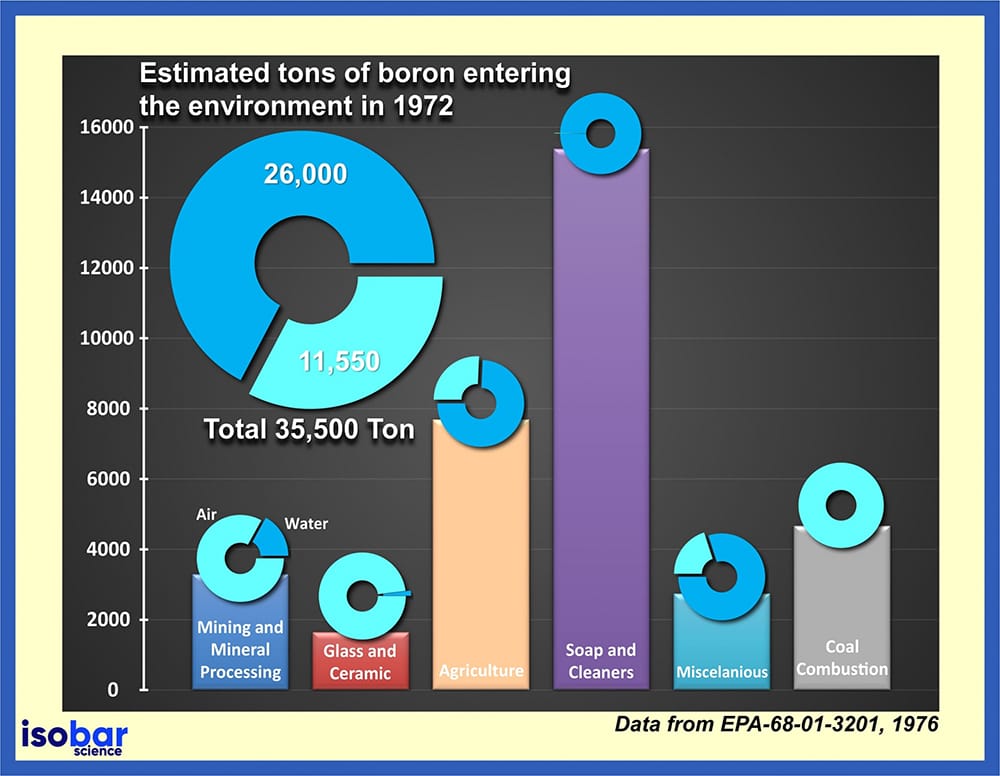
Estimativa de toneladas de boro introduzidas no meio ambiente desde 1972 (Dados da EPA-68-01-3201,1976).
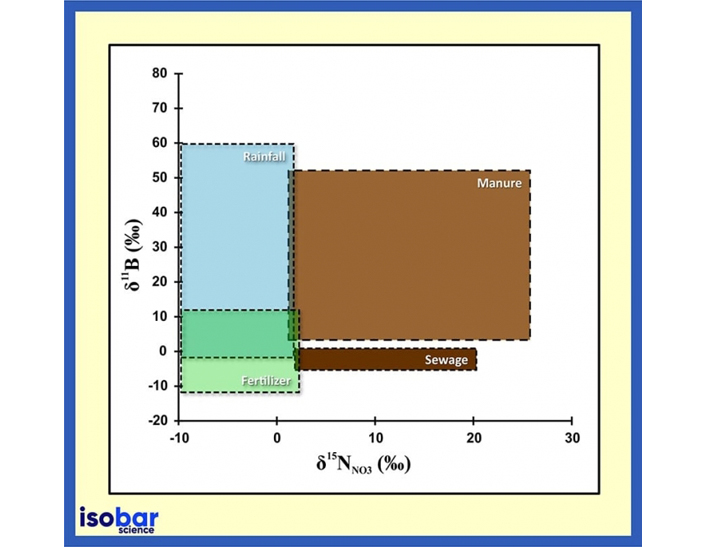
Assinatura de fonte de boro e razões isotópicas de nitrogênio em água (Briand et al., 2013).
Devido à ampla utilização do boro em tantos e diversos produtos, ele acaba sendo liberado no meio ambiente de forma frequente. Com base em dados proporcionados pela Agência de Proteção Ambiental dos Estados Unidos (EPA, 1976), apenas em 1972 um total de 35,5 quilotoneladas de boro foi lançado no meio ambiente, do qual 73% foram introduzidos diretamente na água. A liberação de boro é particularmente problemática, pois não só o boro não pode ser destruído no meio ambiente, como ele muda sua forma ao separar-se e agregar-se a outras partículas em solos, sedimentos e águas. Esse boro pode eventualmente chegar em alimentos (vegetais e frutas), já que é um nutriente essencial para o crescimento das plantas.
Referências
Briand, C., Plagnes, V., Sebilo, M., Louvat, P., Chesnot, T., Schneider, M., Ribstein, P. and Marchet, P., (2013). Combination of nitrate (N, O) and boron isotopic ratios with microbiological indicators for the determination of nitrate sources in karstic groundwater. Environmental Chemistry, 10(5), pp.365-369. DOI: 10.1071/EN13036
Chalk, T.B., Foster, G.L. and Wilson, P.A., (2019). Dynamic storage of glacial CO2 in the Atlantic Ocean revealed by boron [CO32−] and pH records. Earth and Planetary Science Letters, 510, pp.1-11. DOI: 10.1016/j.epsl.2018.12.022
EPA (Environmental Protection Agency), (1976). Chemical technology and economics in environmental perspectives. Task II- Removal of Boron from wastewater. Environmental Protection Agency, Office of Toxic Substances, Washington, D.C. 20460
Giri, S.J., Swart, P.K. and Pourmand, A., (2019). The influence of seawater calcium ions on coral calcification mechanisms: Constraints from boron and carbon isotopes and B/Ca ratios in Pocillopora damicornis. Earth and Planetary Science Letters, 519, pp.130-140. DOI: 10.1016/j.epsl.2019.05.008
Martínez-Botí, M.A., et al. (2015). Boron isotope evidence for oceanic carbon dioxide leakage during the last deglaciation. Nature, 518(7538), pp.219-222. DOI: 10.1038/nature14155

