鍶(Sr)地球化學概論
鍶元素有四個天然的同位素: 84Sr, 86Sr, 87Sr, and 88Sr。只有87Sr是放射性的–由87銣經β-衰變而來,其半衰期為4880萬年。豐度最高的鍶同位素是88Sr,在自然界的出現比例高達83%; 其他的鍶同位素豐度依序為10% 86Sr, 7% 87Sr and <1% 84Sr。在地質和環境調查中,最常使用 87Sr/86Sr比值,因為它們的豐度很接近 – 分別為7%和10%。
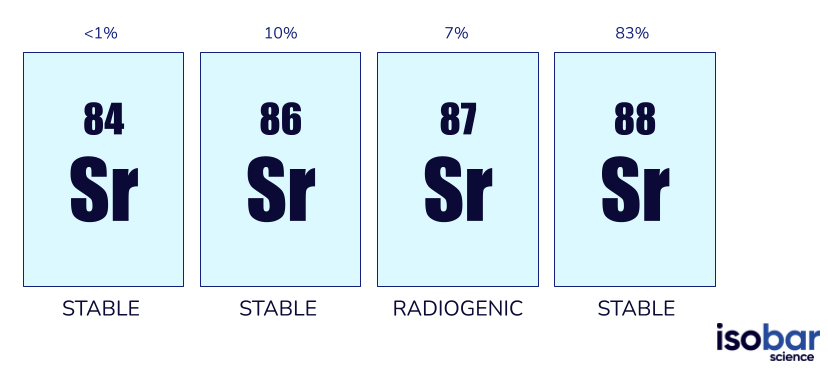
四種鍶同位素。87Sr/86Sr比值通常用於地球化學研究。
鍶是一種微量元素,存在於岩石、土壤、水、植物和動物等各種物質中。87Sr/86Sr比值 與地球化學成因、銣濃度和原岩年齡呈函數關係。因為鍶的質量比較大,鍶的同位素比值基本上不會因岩石風化、流水搬運以及食物鏈等過程而改變。所以 87Sr/86Sr 比值廣泛地使用於地球化學指紋、來源追蹤、汙染預測、以及遷移/流動等研究。海水中 87Sr/86Sr 比值隨時間的系統變化為海洋生物碳酸鹽和磷酸鹽的鍶地層學和鍶年代學提供了研究基礎。
更多關於可進行鍶分析的Sample Types and Selection 樣品類型與取樣資訊。
考古學
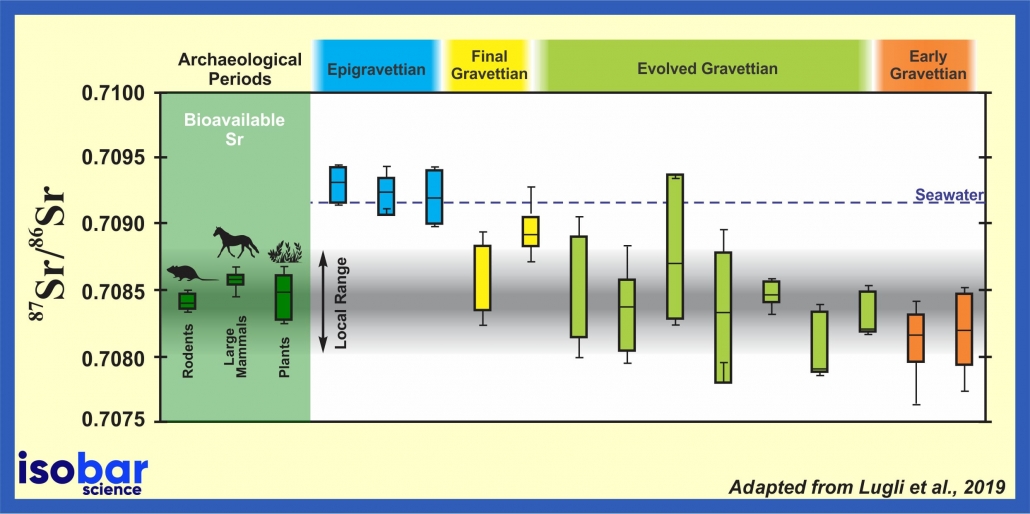
人類乳牙的鍶同位素比 (87Sr/86Sr) 研究顯示了在 Gravettian 和 Epigravettian 時代(32157-19097 yr cal BP)最後一次冰河時期期間人類在意大利南部的移動情形。摘錄自Lugli et al., 2019.
世界上每個地區都會根據周圍的地質和水源呈現特定的 87Sr/86Sr比值。地質和土壤的 87Sr/86Sr比值特徵則與其來源相關。因此,人類、植物和其他動物承繼了它們棲息地的鍶同位素特徵,因為鍶與其他元素會一併被吸收到它們的細胞中(例如: 鈣元素)。
當人類與動物從一個棲息地遷移到另一個棲息地時,他們會接觸不同來源的水和食物(植物及動物)。量測人類及動物的骨頭和頭髮的87Sr/86Sr比值在追蹤遷移與移動方面是一種強而有力的工具。例如,分析人類牙齒的87Sr/86Sr可以提供出生地的資訊,這是由於人類出生時乳齒與恆齒就已經形成了。此外,像是頭髮和指甲這一類會不斷生長,它們的 87Sr/86Sr也不斷更新,則能提供死亡前的生活據點的證據。
閱讀其他文章:
地下水
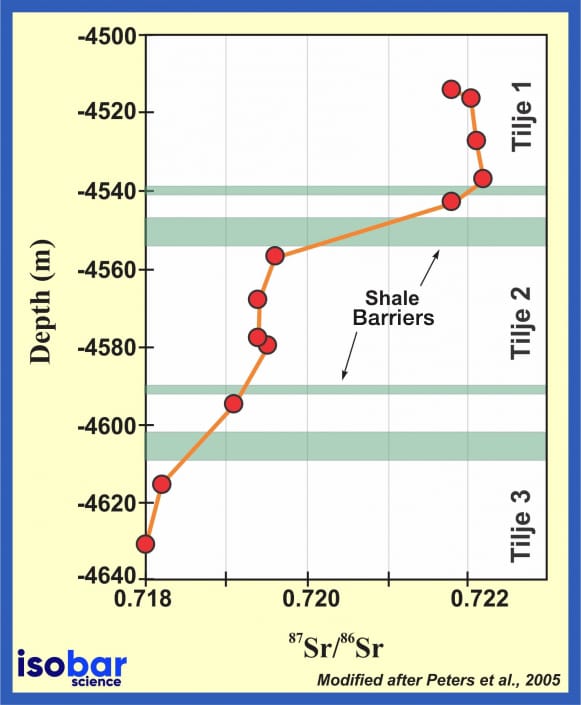
物理風化過程並不會影響鍶同位素比值。既然 87Sr/86Sr比值不受物理風化影響,其比值就反映了周圍岩石形成初始的數值,因此也可以用以分析岩石風化種類。
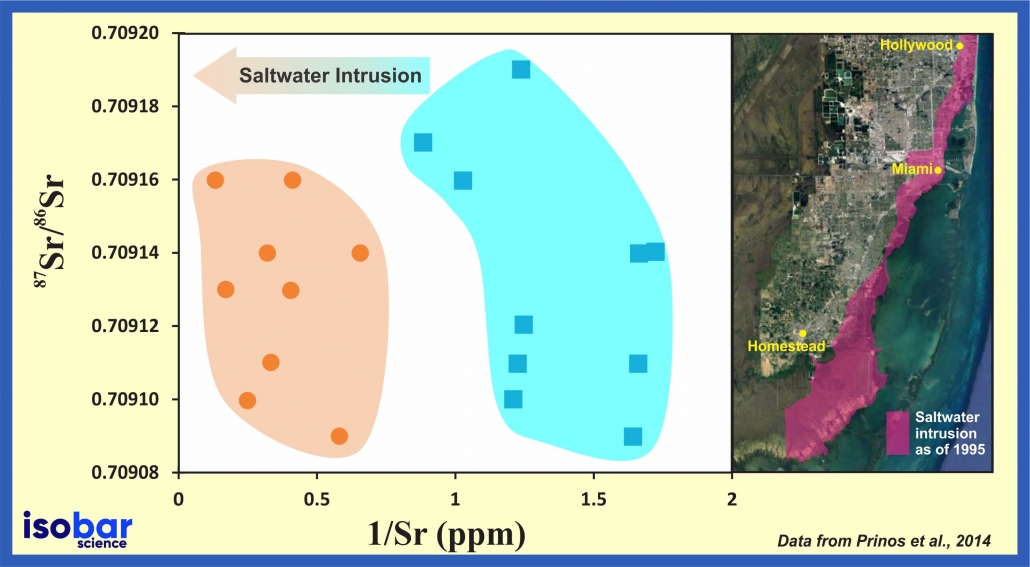
此外,地下水的87Sr/86Sr比值也反應了水源加上流經岩層的同位素特徵。對於追蹤地下水的混合與污染而言,如鹹水入侵,使用水體鍶同位素比值加上鍶濃度的數據是一種有效的方法。
例如,使用鍶濃度與其同位素比值畫出的地下水圖譜,可用於追蹤地下水汙染源與汙染程度,請參閱Nigro et al. (2017)的解說
閱讀更多關於 風化過程中的鍶-釹(Sr-Nd)同位素變化研究.
地質年代學和地層學
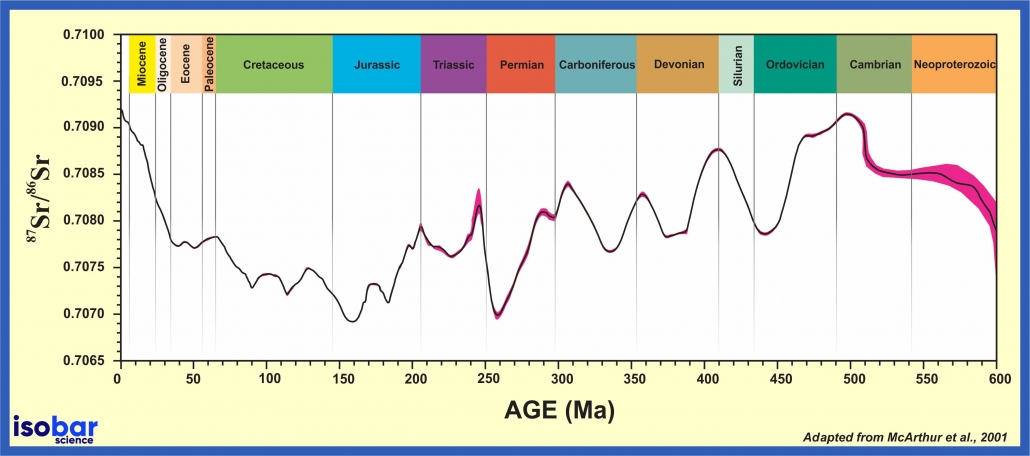
地質年代裡的鍶同位素比值( 87 Sr/ 86 Sr)數據則需藉由分析世界各地的塊體沉積物、未變質的腕足動物、箭石、牙形石與有孔蟲等樣品來取得。紅色區域表示95%的可信任區間。編輯自McArthur et al., 2001.
海洋生物碳酸鹽和磷酸鹽的沉澱牽涉到從海水中吸收鍶,所以其87Sr/86Sr比值與形成時的海水值相同。海洋的87Sr/86Sr比值會隨時間而改變,創造出可預期的曲線,可用於定年計算。這個海水鍶同位素曲線可建立過去8億5千萬年以來的變化,分別使用有孔蟲的碳酸鹽、箭石外殼、菊石文石、環礁的碳酸鹽和海洋膠結物等分析而得(McArthur et al. 2012)。
藉由測量樣品的87Sr/86Sr比值,並比對海水鍶同位素標準曲線,便可獲得樣品(海洋礦物)的年齡。這種方法最適用於 87Sr/86Sr比值長期單向變化的時間段,例如第三紀,但技術上可以應用的年代超過 6 億年。這種方法的最大時間分辨率為 100 萬年。
法醫學
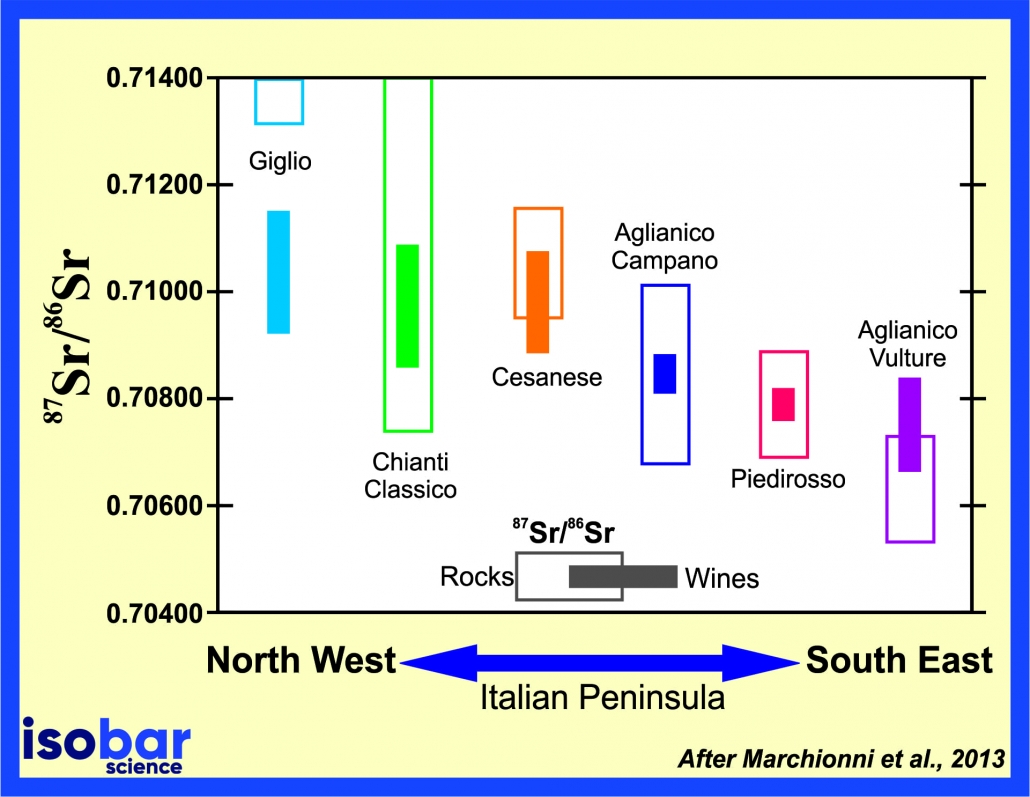
俗話說”人如其食”,生物體內的同位素特徵也是一樣的。人類、植物及其他動物的細胞反應了生活環境中食物與水的同位素標記,包含 87Sr/86Sr。這種標記已成功地用於法醫學中的毒品地球化學指紋識別、研究在社會群體生活下個人的種族背景、追蹤社群的遷移模式、查明死亡地點和追蹤食品摻假,尤其是在葡萄酒業。考古學在研究早期文明的人口遷移、貨物貿易和生活方式特徵方面,也使用類似的技術。
歡迎到我們的部落格閱讀更多:
參考文獻
Bentley, R.A., (2006). Strontium isotopes from the earth to the archaeological skeleton: a review. Journal of archaeological method and theory, 13(3), pp.135-187. DOI: 10.1007/s10816-006-9009-x
Capo, R.C., Stewart, B.W. and Chadwick, O.A., (1998). Strontium isotopes as tracers of ecosystem processes: theory and methods. Geoderma, 82(1-3), pp.197-225. DOI: 10.1016/S0016-7061(97)00102-X
Lugli, F., Cipriani, A., Capecchi, G., Ricci, S., Boschin, F., Boscato, P., Iacumin, P., Badino, F., Mannino, M.A., Talamo, S. and Richards, M.P., (2019). Strontium and stable isotope evidence of human mobility strategies across the Last Glacial Maximum in southern Italy. Nature ecology & evolution, 3(6), pp.905-911. DOI: 10.1038/s41559-019-0900-8
Marchionni, S., Braschi, E., Tommasini, S., Bollati, A., Cifelli, F., Mulinacci, N., Mattei, M. and Conticelli, S., (2013). High-precision 87Sr/86Sr analyses in wines and their use as a geological fingerprint for tracing geographic provenance. Journal of agricultural and food chemistry, 61(28), pp.6822-6831. DOI: 10.1021/jf4012592
McArthur, J.M., Howarth, R.J. and Bailey, T.R., (2001). Strontium isotope stratigraphy: LOWESS version 3: best fit to the marine Sr-isotope curve for 0–509 Ma and accompanying look-up table for deriving numerical age. The Journal of Geology, 109(2), pp.155-170. DOI: 10.1086/319243
McArthur, J.M., Howarth, R.J. and Shields, G.A., 2012. Strontium isotope stratigraphy. The geologic time scale, 1, pp.127-144.
Nigro, A., Sappa, G. and Barbieri, M., (2017). Strontium isotope as tracers of groundwater contamination. Procedia Earth and Planetary Science, 17, pp.352-355. DOI: 10.1016/j.proeps.2016.12.089
Peters, K.E., Walters, C.C. and Moldowan, J.M., (2007). The biomarker guide: Volume 1, Biomarkers and isotopes in the environment and human history. Cambridge university press.
Prinos, S.T., Wacker, M.A., Cunningham, K.J. and Fitterman, D.V., (2014). Origins and delineation of saltwater intrusion in the Biscayne aquifer and changes in the distribution of saltwater in Miami-Dade County, Florida (No. 2014-5025). US Geological Survey. DOI: 10.3133/sir20145025